Patologías del Sistema Nervioso
El cerebro humano — 86 mil millones de neuronas conectadas por billones de sinapsis — es quizás la estructura más compleja del universo conocido. Pero esa complejidad tiene un precio: cuando algo falla, las consecuencias pueden ser devastadoras. Las enfermedades neurológicas y psiquiátricas representan la mayor carga de discapacidad a nivel mundial, afectando a más de mil millones de personas.
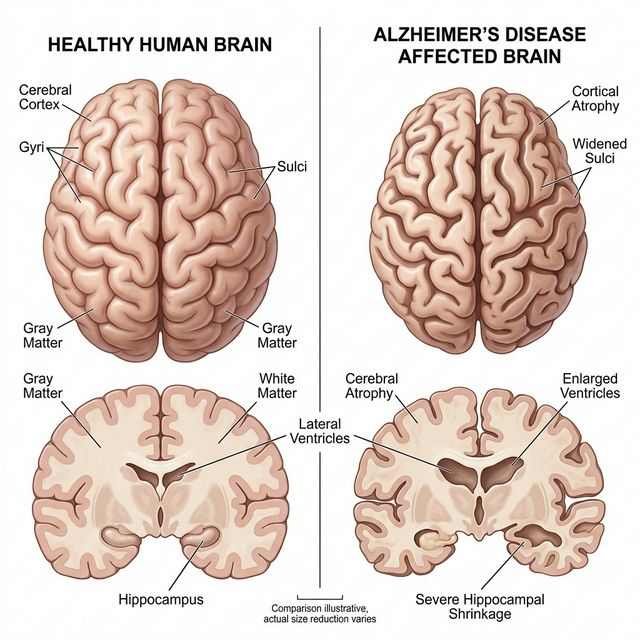
Enfermedad de Alzheimer
El Alzheimer es la causa más común de demencia, representando el 60-80% de los casos. Su patología se caracteriza por dos procesos moleculares interconectados:
- Placas de beta-amiloide (Aβ): La proteína precursora de amiloide (APP) se corta de forma anormal por las enzimas β-secretasa y γ-secretasa, generando fragmentos de Aβ42 que se agregan fuera de las neuronas formando placas insolubles. Estas placas desencadenan una respuesta inflamatoria crónica mediada por la microglía, dañando las sinapsis circundantes.
- Ovillos neurofibrilares de tau: Dentro de las neuronas, la proteína tau — que normalmente estabiliza los microtúbulos del citoesqueleto — se hiperfosforila y colapsa en ovillos enredados. Sin microtúbulos funcionales, el transporte axonal cesa y la neurona muere.
- Muerte hipocampal: El hipocampo es la primera región atacada, explicando por qué la pérdida de memoria episódica es el síntoma inicial. A medida que la patología se extiende a la corteza temporal, parietal y frontal, emergen déficits en lenguaje, orientación espacial y funciones ejecutivas.
La hipótesis de la cascada amiloide propone que Aβ es el evento iniciador, pero evidencia reciente sugiere que tau, neuroinflamación y disfunción sináptica son mediadores críticos del daño cognitivo. De hecho, pacientes con alta carga amiloide pero baja tau pueden permanecer cognitivamente normales durante años.
Enfermedad de Parkinson
El Parkinson resulta de la muerte progresiva de neuronas dopaminérgicas en la sustancia negra pars compacta (SNpc). Estas neuronas son esenciales para la vía nigroestriatal, que modula los ganglios basales.
- Fisiopatología: Sin dopamina suficiente, la vía directa (facilitadora del movimiento) se debilita y la vía indirecta (inhibitoria) domina. El resultado es un estado de excesiva inhibición tálamo-cortical.
- Síntomas cardinales: Temblor en reposo (4-6 Hz, típicamente en “contar monedas”), rigidez (“rueda dentada”), bradicinesia (lentitud de movimiento) y inestabilidad postural.
- Cuerpos de Lewy: Agregados intracelulares de la proteína α-sinucleína, presentes en las neuronas afectadas. Se propone que la α-sinucleína patógena se propaga de célula a célula de manera “priónica”.
Los síntomas motores aparecen cuando ya se ha perdido el 60-80% de las neuronas dopaminérgicas, lo que subraya la importancia de la detección precoz mediante biomarcadores.
Depresión Mayor
La depresión es mucho más que “estar triste”. Es un trastorno neurobiológico con alteraciones medibles en la estructura y función cerebral:
- Hipótesis monoaminérgica: Déficit funcional de serotonina (5-HT), noradrenalina y/o dopamina en circuitos límbicos y corticales. Esta hipótesis explica por qué los ISRS (Inhibidores Selectivos de la Recaptación de Serotonina) son efectivos, aunque su latencia de semanas sugiere mecanismos más complejos.
- Neurogénesis reducida: El estrés crónico, a través del cortisol elevado, reduce la neurogénesis en el giro dentado del hipocampo. Los antidepresivos y el ejercicio físico promueven la neurogénesis, correlacionando con la mejora clínica.
- Hipoactividad prefrontal: La corteza prefrontal dorsolateral (dlPFC) muestra actividad reducida, comprometiendo la regulación emocional top-down. Simultáneamente, la amígdala y la red de modo predeterminado (DMN) muestran hiperactividad, asociada a rumia y sesgo negativo.
- Vía glutamatérgica: La ketamina, un antagonista NMDA, produce efectos antidepresivos rápidos (horas vs semanas), sugiriendo que la disfunción glutamatérgica y la plasticidad sináptica son piezas clave del rompecabezas.
Trastornos del Neurodesarrollo: TEA y TDAH
El Trastorno del Espectro Autista (TEA) y el Trastorno por Déficit de Atención e Hiperactividad (TDAH) comparten raíces en alteraciones de la conectividad cerebral durante el desarrollo:
- TEA — Diferencias de conectividad: Existe una combinación de hiperconectividad local (exceso de conexiones dentro de redes sensoriales) e hipoconectividad de larga distancia (déficit de conexiones entre regiones distantes, especialmente entre corteza frontal y áreas temporoparietales). Esto puede explicar la hipersensibilidad sensorial y las dificultades en integración social.
- TDAH — Circuito prefrontal-estriatal: La disfunción de la vía dopaminérgica mesocortical que conecta el área tegmental ventral con la corteza prefrontal produce déficits en atención sostenida y funciones ejecutivas. La vía nigroestriatal alterada contribuye a la hiperactividad motora. Los estimulantes como el metilfenidato aumentan la dopamina y noradrenalina en PFC, mejorando el control atencional.
- Base genética: Ambos trastornos son altamente heredables (TEA ~80%, TDAH ~75%). Involucran cientos de genes de efecto pequeño que afectan la sinaptogénesis, la poda sináptica y la señalización dopaminérgica.
Neurotecnología: La Frontera entre Biología y Silicio
La neurotecnología engloba todas las herramientas que permiten registrar, interpretar, modular o reemplazar funciones del sistema nervioso. Estamos viviendo una revolución sin precedentes en tres frentes principales.
Interfaces Cerebro-Máquina (BMI/BCI)
Una interfaz cerebro-máquina traduce la actividad neuronal en comandos para dispositivos externos, creando un puente directo entre la intención mental y la acción física:
- BrainGate (Utah Array): Un microarray de 96 electrodos de silicio (4x4 mm) implantado en la corteza motora primaria (M1). Registra los potenciales de acción de neuronas individuales mientras el paciente imagina movimientos. Algoritmos de decodificación traducen estos patrones neurales en movimiento de cursores, brazos robóticos o texto en pantalla. La precisión alcanza el 94% en tareas de escritura imaginada.
- EEG-BCI (no invasiva): Utiliza electroencefalografía desde el cuero cabelludo. Menor resolución espacial pero sin riesgos quirúrgicos. Aplicaciones incluyen sillas de ruedas controladas por pensamiento, comunicadores para pacientes con síndrome de enclaustramiento, y sistemas de neuro-feedback para rehabilitación post-ictus.
- Neuralink y electrodos flexibles: La nueva generación busca resolver el problema de la “cicatriz glial” — la respuesta inflamatoria del cerebro que degrada los electrodos rígidos. Los electrodos ultrafinos y flexibles prometen interfaces estables durante décadas.
Neuromodulación
Más allá de leer el cerebro, podemos escribir en él:
- Estimulación Cerebral Profunda (DBS): Electrodos implantados quirúrgicamente en estructuras específicas (núcleo subtálamico, globo pálido interno) envían pulsos eléctricos continuos de alta frecuencia (130 Hz). Invasiva pero extraordinariamente efectiva: elimina el temblor parkinsoniano en segundos, trata la depresión resistente y el TOC severo. El mecanismo exacto sigue en debate — probablemente modula patrones oscilatorios patológicos más que simplemente “estimular” o “inhibir”.
- Estimulación Magnética Transcraneal (TMS): Un electroimán externo genera pulsos magnéticos que inducen corrientes eléctricas en la corteza subyacente. No invasiva, sin cirugía, aplicada desde fuera del cráneo. La TMS repetitiva (rTMS) de la dlPFC está aprobada por la FDA para depresión resistente a fármacos. Frecuencias altas (~10 Hz) excitan; frecuencias bajas (~1 Hz) inhiben.
- Estimulación transcraneal por corriente directa (tDCS): Una corriente débil (1-2 mA) modula la excitabilidad cortical. Barata, portátil y no invasiva, aunque con efectos más sutiles.
Neuroimagen
Ver dentro del cerebro vivo ha transformado la neurociencia:
- fMRI (Resonancia Magnética Funcional): Mide cambios en el flujo sanguíneo cerebral (señal BOLD) como proxy de la actividad neuronal. Excelente resolución espacial (~1-2 mm) pero temporal limitada (~2 s). Permite mapear redes funcionales, localizar tumores prequirúrgicamente y estudiar la conectividad funcional en reposo.
- PET (Tomografía por Emisión de Positrones): Utiliza radiotrazadores para visualizar procesos bioquímicos específicos: metabolismo de glucosa (FDG-PET), depósitos de amiloide (PiB-PET), densidad de receptores dopaminérgicos. Es la única técnica que puede “ver” moléculas específicas in vivo.
- MEG (Magnetoencefalografía): Detecta los campos magnéticos ultradébiles generados por corrientes iónicas neuronales. Combina excelente resolución temporal (milisegundos) con buena localización espacial. Ideal para mapear la dinámica temporal de las oscilaciones cerebrales y localizar focos epilépticos.

El Futuro del Cerebro
Las tecnologías que acabamos de estudiar nos sitúan en el umbral de preguntas que antes pertenecían exclusivamente a la ciencia ficción. Cuatro fronteras definen el horizonte de la neurociencia del siglo XXI.
Aumento Cognitivo
¿Podemos mejorar un cerebro sano? Ya lo hacemos, en cierta medida. La cafeína mejora la vigilancia, el modafinilo la atención sostenida, y la tDCS puede incrementar la velocidad de aprendizaje motor. Pero los límites se difuminan rápidamente:
- Nootrópicos farmacológicos: Fármacos diseñados para potenciar la memoria de trabajo, la consolidación mnemónica o la creatividad. Las moléculas que potencian la señalización CREB en el hipocampo podrían mejorar la formación de memorias a largo plazo.
- Estimulación no invasiva: Protocolos de tDCS y TMS optimizados para mejorar funciones cognitivas específicas en individuos sanos. ¿Dónde termina la “terapia” y comienza el “aumento”?
Prótesis Neurales
Más allá de las interfaces motoras, se desarrollan prótesis para funciones cognitivas:
- Prótesis hipocampal: Theodore Berger (USC) ha demostrado en roedores y primates que un chip de silicio puede replicar la transformación de memoria de corto a largo plazo que realiza el hipocampo, restaurando la capacidad de formar nuevos recuerdos tras daño hipocampal.
- Implantes cocleares y retinales: Ya son realidad clínica. El implante coclear es la neuroprótesis más exitosa de la historia, con más de un millón de usuarios. Los implantes retinales (Argus II) restauran visión básica en retinitis pigmentosa.
Inteligencia Artificial y Neurociencia
La relación entre IA y neurociencia es bidireccional y cada vez más fructífera:
- IA inspirada en el cerebro: Las redes neuronales profundas (Deep Learning) surgieron de modelos del procesamiento visual cortical (Hubel y Wiesel). Las redes recurrentes modelan memoria a corto plazo; los transformers replican mecanismos atencionales.
- IA como herramienta neurocientífica: Algoritmos de machine learning decodifican patrones de fMRI, predicen el curso de enfermedades neurodegenerativas y descubren biomarcadores en datos masivos que escapan al análisis humano.
- Convergencia: Los modelos computacionales del cerebro se vuelven cada vez más sofisticados. El proyecto Human Brain Project (Europa) y BRAIN Initiative (EE.UU.) buscan crear simulaciones completas de circuitos cerebrales.
El Problema Difícil de la Conciencia
Todas las tecnologías anteriores convergen en la pregunta más profunda de la neurociencia: ¿cómo genera la materia física la experiencia subjetiva?
- El problema fácil vs el difícil (Chalmers, 1995): El problema “fácil” es explicar los mecanismos funcionales (cómo el cerebro discrimina estímulos, integra información, genera reportes verbales). El problema “difícil” es por qué existe una experiencia subjetiva asociada a estos procesos — por qué “hay algo que es como” ser consciente.
- Teoría de la Información Integrada (IIT): Propuesta por Giulio Tononi, sugiere que la conciencia es idéntica a la información integrada (Φ) — la cantidad de información generada por un sistema como un todo, por encima de sus partes.
- Teoría del Espacio de Trabajo Global (GNW): Propuesta por Dehaene y Changeux, sostiene que la conciencia surge cuando la información se “difunde” a través de una red frontoparietal de neuronas con axones largos, haciéndola accesible globalmente.
- Implicaciones: Si la conciencia depende de la estructura computacional (como sugiere IIT), entonces un sustrato de silicio suficientemente complejo podría ser consciente. Si depende del sustrato biológico específico, ninguna máquina lo será.
Caso Clínico: BrainGate — Escribir con el pensamiento
En 2021, un paciente varón de 65 años con Esclerosis Lateral Amiotrófica (ELA) — una enfermedad que destruye las neuronas motoras inferiores, paralizando progresivamente todos los músculos voluntarios — recibió un implante BrainGate (Utah Array) en su corteza motora primaria (M1). Aunque su cuerpo estaba casi completamente paralizado, su cerebro seguía intacto. Los investigadores le pidieron que imaginara escribir letras a mano con un lápiz imaginario. Los electrodos registraron la actividad de ~200 neuronas de M1, y un algoritmo de red neuronal recurrente (RNN) decodificó los patrones de actividad en letras individuales.
El resultado fue extraordinario: el paciente logró escribir texto a 90 caracteres por minuto con una precisión del 94.1% en tiempo real (99% con autocorrección). Esta velocidad se aproxima a la velocidad de escritura típica en un smartphone para personas de su edad (~115 caracteres/min), y superó ampliamente cualquier BCI anterior.
La clave: neuronas motoras superiores vs inferiores.
La ELA destruye las neuronas motoras inferiores en la médula espinal y el tronco encefálico — las que conectan directamente con los músculos. Sin embargo, las neuronas motoras superiores en M1 (corteza motora primaria) permanecen funcionales durante gran parte de la enfermedad.
Cuando el paciente imagina escribir una letra, las neuronas de M1 generan el mismo patrón de actividad que generarían si el movimiento fuera real. BrainGate “intercepta” estas señales antes de que desciendan por el tracto corticoespinal dañado, decodificándolas directamente desde la corteza.
Cada letra tiene un patrón único: Las trayectorias imaginadas de cada letra producen patrones neurales espaciotemporales distintos — la “a” activa un conjunto diferente de neuronas en una secuencia diferente a la “b”. El algoritmo RNN aprende estas “firmas neurales” durante una fase de entrenamiento de solo unos minutos.
Este caso demuestra un principio fundamental: la intención motora es computación cortical, independiente de la ejecución muscular. BrainGate no cura la parálisis — la rodea.